Lösungsansätze von Bausch+Ströbel
 Die Umsetzung der Annex-1-Anforderungen ist in der Praxis oft komplex. Sterile Produktionsprozesse stehen vor Herausforderungen wie kontaminationsfreie Luftströmungen aufrechtzuerhalten, kritische Eingriffe zu minimieren, Reinräume effizient zu überwachen und gleichzeitig Regelkonformität und Prozesssicherheit zu gewährleisten. Auch die Integration von Barrieresystemen, Automatisierung und qualifiziertem Personal stellt viele Unternehmen vor organisatorische und technische Hürden.
Die Umsetzung der Annex-1-Anforderungen ist in der Praxis oft komplex. Sterile Produktionsprozesse stehen vor Herausforderungen wie kontaminationsfreie Luftströmungen aufrechtzuerhalten, kritische Eingriffe zu minimieren, Reinräume effizient zu überwachen und gleichzeitig Regelkonformität und Prozesssicherheit zu gewährleisten. Auch die Integration von Barrieresystemen, Automatisierung und qualifiziertem Personal stellt viele Unternehmen vor organisatorische und technische Hürden.Unsere Abfüll- und Verschlusssysteme sind speziell dafür entwickelt, diese Herausforderungen zu meistern. Mit RABS- und Isolatortechnologie, optimierten First-Air-Konzepten, voll integrierten Environmental-Monitoring-Lösungen und automatisierten Prozessen reduzieren wir menschliche Eingriffe auf ein Minimum. Gleichzeitig unterstützen unsere Systeme QRM- und CCS-Strategien durch lückenlose Dokumentation, validierte Prozesse und kontinuierliche Überwachung.
So verbinden wir Regelkonformität, Sicherheit und Effizienz: Ihre Produktion erfüllt nicht nur die strengen Vorgaben des Annex 1, sondern wird gleichzeitig robuster, zuverlässiger und zukunftssicher.
Ohne Sortiertöpfe. Kontaminationsfrei.
Die nächste Generation der Stopfenzuführung.
Die phar mazeutische Industrie steht durch die verschärften Anforderungen des Annex-1 vor neuen Herausforderungen. Besonders ununterbrochene Luftströmungen (First Air) und die vollständige Sterilisierbarkeit aller produktberührenden Teile setzen traditionelle Stopfenzuführungen mit Sortiertöpfen zunehmend unter Druck. Klassische Systeme verursachen Störungen der First Air, bergen Kontaminationsrisiken und erschweren Reinigung sowie Autoklavierung.
mazeutische Industrie steht durch die verschärften Anforderungen des Annex-1 vor neuen Herausforderungen. Besonders ununterbrochene Luftströmungen (First Air) und die vollständige Sterilisierbarkeit aller produktberührenden Teile setzen traditionelle Stopfenzuführungen mit Sortiertöpfen zunehmend unter Druck. Klassische Systeme verursachen Störungen der First Air, bergen Kontaminationsrisiken und erschweren Reinigung sowie Autoklavierung.Die Antwort: Unsere Lösung einer Stopfenzuführung ohne Sortiertopf
Mit dem Aseptic Bowl-Free-Feed (BFF) haben wir eine zukunftssichere Lösung entwickelt, die Sortiertöpfe vollständig eliminiert – für maximale Sterilität, vereinfachte Prozesse und höchste Automatisierung.
Ihre Vorteile auf einen Blick
- Kompatibilität für alle Arten von Stopfen für Vials, Spritzen und Karpulen
- Hohe Geschwindigkeit – verarbeitet bis zu 60.000 Stopfen pro Stunde und sorgt für maximale Effizienz
- Hygienisches Design für einfache Reinigbarkeit – magnetische Technologie ermöglicht eine gründliche Reinigung
- Reduzierung manueller Eingriffe durch robotergestützte Systeme
- Automatische aseptische Einrichtung möglich
- Zero-Reject-Prinzip für eine maximale Ausbringung
Future-Proof für sterile Pharmazeutika
Der BFF löst zentrale Herausforderungen der aseptischen Herstellung: Er verbessert regulatorische Sicherheit, senkt Kontaminationsrisiken und steigert Effizienz. Durch die Kombination von Robotik und modernstem Hygienic Design setzt er einen neuen Standard für sterile Stopfenzuführung – und macht pharmazeutische Abfüll- und Verschließanlagen bereit für die Anforderungen von morgen.
Continuous Monitoring
 Der überarbeitete EU GMP Annex 1 stellt klare Anforderungen an die kontinuierliche Überwachung von Partikeln sowie weiteren kritischen Parametern während der gesamten Betriebsdauer aseptischer Prozesse. Besonders die mikrobiologische Umweltüberwachung muss lückenlos, reproduzierbar und ohne Beeinträchtigung der Produktion erfolgen.
Der überarbeitete EU GMP Annex 1 stellt klare Anforderungen an die kontinuierliche Überwachung von Partikeln sowie weiteren kritischen Parametern während der gesamten Betriebsdauer aseptischer Prozesse. Besonders die mikrobiologische Umweltüberwachung muss lückenlos, reproduzierbar und ohne Beeinträchtigung der Produktion erfolgen.Um diese Anforderungen zuverlässig und effizient umzusetzen, bieten wir ein vollautomatisches Settle Plate Wechsler zur Verarbeitung sämtlicher Sedimentationsplatten.
Unser System ermöglicht die Integration einer durchgängigen mikrobiologischen Überwachung, bei der die Handhabung der Sedimentationsplatten vollständig automatisiert erfolgt. Dadurch wird das Bedienpersonal während der laufenden Produktion entlastet und menschliche Eingriffe in kritischen Bereichen werden auf ein Minimum reduziert.
Ihre Vorteile auf einen Blick
- Optimale First-Air Immersion
- Zuverlässig dank automatisierter Handhabung: Reduziert menschliche Eingriffe und minimiert das Kontaminationsrisiko
- Kein Vertauschen von beprobten und unbeprobten Sedimentationsplatten: Klare Prozesslogik und eindeutige Zuordnung sorgen für vollständige Rückverfolgbarkeit
- Geeignet für die Verarbeitung von HPAPI: Sicherer Einsatz auch in hochpotenten Wirkstoffumgebungen
Gloveless Lösungen
Der überarbeitete Annex 1 verschärft die Anforderungen an Sterilität und Prozesssicherheit in der aseptischen Produktion deutlich. Jeder menschliche Eingriff gilt als Risiko – selbst über Isolatorhandschuhe. Diese können ermüden, beschädigt werden oder unbemerkt undicht sein und bleiben damit eine Schwachstelle in automatisierten Anlagen.Gloveless-Lösungen beseitigen dieses Risiko, indem sie vollständig auf Handschuhe verzichten und geschlossene, automatisierte Prozesse ermöglichen. So sinkt das Kontaminationsrisiko erheblich, während standardisierte und reproduzierbare Abläufe gewährleistet bleiben. In Verbindung mit Robotik, Sensorik und datenbasiertem Monitoring entsteht ein neues Niveau an stabiler, sicherer Asepsis – optimal für Annex 1 und die Zukunft der sterilen Produktion.
GENEX: Die nächste Generation der handschuhlosen Abfüllung

GENEX ist eine vollständig handschuhlose Prozesslösung speziell für die aseptische Kleinchargenfertigung. Sie wurde entwickelt, um Kontaminationsrisiken signifikant zu reduzieren. Durch den konsequenten Einsatz von Robotik ersetzt GENEX alle manuellen Eingriffe in kritischen Prozessschritten wie Handling, Befüllung, Stopfen und Crimpen. So werden menschliche Fehler vermieden und die Anforderungen von EU-GMP Annex 1 und FDA-Richtlinien zuverlässig erfüllt.
Die Plattform ist modular, skalierbar und äußerst kompakt – ideal für Biologika, Impfstoffe und ATMPs, die absolute Sterilität, schnelle Umrüstungen und minimale Produktverluste verlangen. Angesichts des Branchentrends hin zu hochpreisigen, empfindlichen Therapien in kleinen Chargen schafft GENEX die notwendige Flexibilität: Robotikmodule lassen sich schnell für neue Formate programmieren, und die Anlage kann ohne lange Stillstände umkonfiguriert werden. So verbindet GENEX maximale aseptische Sicherheit mit hoher Agilität.
Vorteile GENEX
- Minimiertes Kontaminationsrisiko dank vollständig robotergesteuertem, gloveless Isolatorbetrieb
- Höchste Flexibilität durch robotergestützte, GMP-konforme Formatwechsel
- Ideal für klinische Studien und Kleinchargen verschiedenster Produktarten und Füllvolumina
- Beschleunigte Zulassungsverfahren dank reproduzierbarer, validierbarer und standardisierter Prozesse
Hygienic Design im Sinne von Annex 1
 Mit der Überarbeitung von EU GMP Annex 1 sind die Anforderungen an das Hygienic Design von Abfüllanlagen für sterile Arzneimittel deutlich gestiegen. Ziel ist es, jede potenzielle Kontaminationsquelle konsequent zu eliminieren und Reinigbarkeit sowie Bio-Dekontamination auf höchstem Niveau sicherzustellen.
Mit der Überarbeitung von EU GMP Annex 1 sind die Anforderungen an das Hygienic Design von Abfüllanlagen für sterile Arzneimittel deutlich gestiegen. Ziel ist es, jede potenzielle Kontaminationsquelle konsequent zu eliminieren und Reinigbarkeit sowie Bio-Dekontamination auf höchstem Niveau sicherzustellen.Ein zentraler Ansatz ist die Überarbeitung unserer Durchtransportes der Objekte. Es befinden sich keine beweglichen Teile in „grauen“ oder undefinierten Zonen. Alle funktionalen Komponenten sind klar definierten, kontrollierbaren Bereichen zugeordnet – eine entscheidende Voraussetzung für Compliance, Risikominimierung und Audit-Sicherheit.
Ein durchgängiges Hygienic Design spielt zudem eine entscheidende Rolle bei der Sicherung der First Air. Strömungsoptimierte Geometrien, reduzierte Bauteilhöhen und das Vermeiden unnötiger Aufbauten stellen sicher, dass kritische Zonen – insbesondere im Füllbereich – jederzeit unter aseptischen Luftstrom bleiben und nicht durch mechanische Komponenten oder Turbulenzen beeinträchtigt werden.
Das Ergebnis ist ein ganzheitliches Anlagenkonzept mit optimaler Reinigbarkeit, effizienter Bio-Dekontamination (z. B. VHP), verkürzten Stillstandszeiten und maximaler Produktsicherheit.
Annex 1 Konformität mit CFD‑Studien
Der EU‑GMP Annex 1 verlangt einen nachweisbaren Schutz des Produkts während kritischer Schritte im aseptischen Füll‑ und Verschließprozess. Ein zentrales Element ist dabei die Einhaltung der sogenannten First‑Air‑Bedingungen im produktnahen Bereich. CFD‑Studien (Computational Fluid Dynamics) liefern hierfür einen belastbaren, simulationsbasierten Nachweis.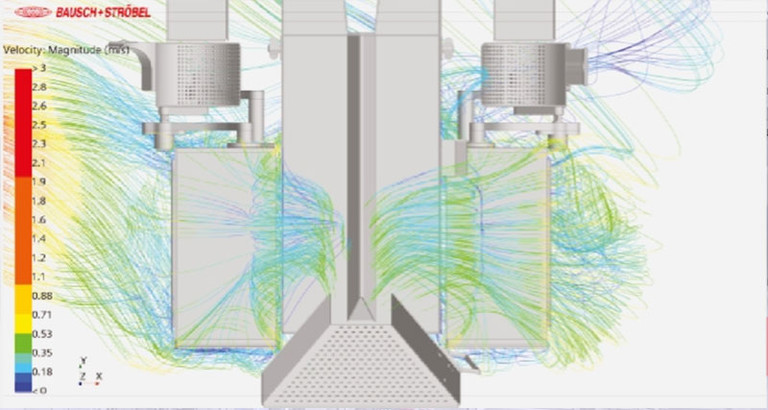
Mithilfe von CFD‑Analysen werden die Luftströmungen im Bereich von Füllnadeln, Stopfensetzung und Verschließstationen detailliert simuliert und visualisiert. Dadurch lässt sich frühzeitig bewerten, ob die geforderte, ungestörte Luftführung zum Produkt hin eingehalten wird und wie sich Maschinendesign, Barrieren oder Druckzonen auf den Produktschutz auswirken.
Ein wesentlicher Vorteil der CFD‑Studien liegt in ihrer frühen Einsetzbarkeit: Bereits in der Design‑, Planungs‑ oder Umbauphase können kritische Bereiche identifiziert und gezielt optimiert werden – noch bevor die Anlage in Betrieb geht. Die Ergebnisse dienen als nachvollziehbare, technisch fundierte Dokumentation und unterstützen Hersteller dabei, Annex‑1‑Anforderungen zur First‑Air‑Führung transparent und belastbar gegenüber Behörden nachzuweisen.
Mit Omnia zur Annex‑1-Compliance
Der EU-GMP Annex 1 fordert eine umfassende und nachvollziehbare Kontrolle aseptischer Füll- und Verschließprozesse über den gesamten Lebenszyklus einer Linie hinweg. Mit Omnia stellt B+S eine digitale Lösung bereit, die Hersteller dabei unterstützt, diese Anforderungen strukturiert und datenbasiert umzusetzen.
Omnia dient als zentrale Plattform zur Erfassung, Auswertung und Dokumentation prozessrelevanter Informationen entlang von Füll- und Verschließlinien. Dazu zählen unter anderem Prozesszustände, Eingriffe, Alarme sowie ausgewählte Umgebungs- und Betriebsparameter in produktnahen Bereichen. Die konsistente Zusammenführung dieser Daten schafft Transparenz über den tatsächlichen Zustand der Linie im Betrieb und ermöglicht eine objektive Bewertung von Abweichungen und Risiken.
Durch standardisierte Auswertungen, klare Visualisierungen und eine revisionssichere Dokumentation unterstützt Omnia fundierte Entscheidungen im laufenden Betrieb und bei Prozessänderungen. Gleichzeitig erleichtert die strukturierte Datenbasis die Vorbereitung und Durchführung von Audits und Inspektionen. So leistet Omnia einen wesentlichen Beitrag zur nachhaltigen Einhaltung der Annex-1-Anforderungen an aseptische Füll- und Verschließprozesse.
PUPSIT – Sicherheit vor Produktionsstart
PUPSIT (Pre-Use-Post-Sterilisation-Integrity-Test) bezeichnet den Filterintegritätstest nach der Sterilisation und unmittelbar vor Produktionsbeginn. Damit wird sichergestellt, dass der finale Produktfilter genau in dem Zustand geprüft wird, in dem er später für die sterile Abfüllung eingesetzt wird.Denn Transport, Installation und Sterilisation können zu Beschädigungen der Filtermembran führen. Früher erfolgte der Integritätstest häufig erst am Ende der Produktion. Man nahm in Kauf, dass ein möglicher Defekt erst nach der Abfüllung erkannt wird. Heute ist jedoch bekannt, dass das Produkt selbst kleinste Schäden kaschieren und das Testergebnis verfälschen kann.
Der PUPSIT gilt inzwischen als wesentlicher Bestandteil eines regulatorisch konformen Produktionsprozesses – idealerweise so nah wie möglich am Point-of-Use durchgeführt, um maximale Produktsicherheit zu gewährleisten.
Wir integrieren das komplette Produktfilter-Setup in das Füllmaschinendesign – nahe am Point-of-Use, innerhalb oder außerhalb des Isolators. Ob Single-Use-Assembly, SOP- oder CIP/SIP-Systeme, einfache oder doppelte Filtration: Die Auslegung erfolgt prozesssicher und anwendungsspezifisch.
Die automatisierte Filtermembranbenetzung mit Produkt, WFI oder Pufferlösung sowie die Auswahl gängiger Testmethoden wie Forward Flow, Bubble Point oder Water Intrusion Test ermöglichen stabile Abläufe unmittelbar vor Produktionsstart – inklusive vollständiger Protokollierung im Batchprotokoll.
Filtertestgeräte aller namhaften Hersteller werden in die Maschinensteuerung integriert, Testergebnisse und Prozessparameter wie Druck und Durchfluss kontinuierlich erfasst. Ergänzend optimieren wir das Filtrationsdesign zur Minimierung von Produktverlusten – sowohl in Neuanlagen als auch bei Bestandsprojekten, unabhängig vom Filtertyp oder Hersteller.
Bestandsanlagen sicher und zukunftsfähig machen
Die Anforderungen des überarbeiteten EU-GMP Annex 1 stellen viele Pharmaunternehmen vor die gleiche Herausforderung: Wie lassen sich bestehende Produktionsanlagen so anpassen, dass sie den verschärften Vorgaben zu Kontaminationskontrolle, Risikomanagement und Barrieretechnologien entsprechen – ohne die laufende Produktion zu gefährden? Wir unterstützen Sie genau an diesen Punkten. Unser Service hilft Ihnen dabei, Ihre Bestandsmaschinen systematisch auf Annex-1-Konformität zu prüfen und notwendige Maßnahmen klar zu definieren. Gemeinsam analysieren wir den aktuellen Anlagenzustand, identifizieren potenzielle Risiken und zeigen konkrete Optimierungs- und Umbauoptionen auf – technisch fundiert, praxisnah und herstellerunabhängig.
Wir unterstützen Sie genau an diesen Punkten. Unser Service hilft Ihnen dabei, Ihre Bestandsmaschinen systematisch auf Annex-1-Konformität zu prüfen und notwendige Maßnahmen klar zu definieren. Gemeinsam analysieren wir den aktuellen Anlagenzustand, identifizieren potenzielle Risiken und zeigen konkrete Optimierungs- und Umbauoptionen auf – technisch fundiert, praxisnah und herstellerunabhängig.Ob kleinere Anpassungen, gezielte Modernisierungen oder umfassende Retrofit-Lösungen: Wir beraten Sie transparent zu allen Möglichkeiten und begleiten Sie von der ersten Bewertung bis zur erfolgreichen Umsetzung. So erhalten Sie eine klare Entscheidungsgrundlage und einen Maßnahmenplan, der Ihre Anlage zuverlässig auf den aktuellen regulatorischen Stand bringt.
Mit uns schaffen Sie die Basis für eine robuste Contamination Control Strategy und langfristige Annex-1-Compliance – effizient, sicher und zukunftsorientiert.
